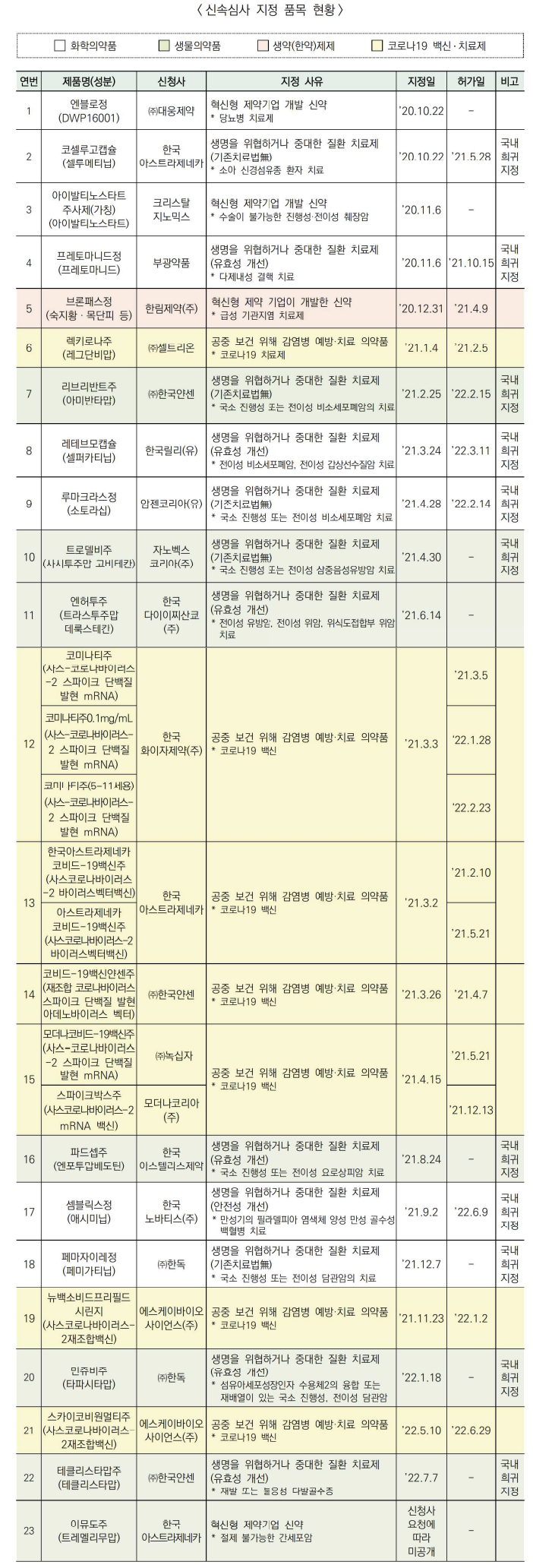
지난 2년 신속심사 23품목 지정...절반이 항악성종양제
국내 1호 지정은 '셀루메티닙' 'DWP16001'
일반심사기간 75% 이내 심사완료 목표... 총 17품목 허가
[데일리팜=이혜경 기자] 지난 2년간 의약품 23품목이 신속심사로 지정됐다. 구체적으로 2020년 4품목, 2021년 11품목, 2022년 7월까지 8품목으로 나타났는데, 지난해 신속지정 의약품이 전년 대비 증가한 이유는 코로나19 백신 영향으로 풀이된다.
식품의약품안전처(처장 오유경)는 국내 혁신 의료제품 개발을 지원하기 위한 '글로벌 혁신제품 신속심사 지원(GIFT) 프로그램'을 본격화하며 '의약품 신속심사 보고서'를 13일 발간했다.
식약처는 지난 2020년 8월 31일부터 신속심사과를 신설하고 생명을 위협하는 질병 또는 희귀·난치질환치료제 등 혁신적 제품 및 공중보건 위기대응 의약품에 대해 신속심사 품목을 지정해 심사하고 있다.
국내에서 처음으로 신속심사로 지정된 품목은 한국아스트라제네카의 '셀루메티닙'과 혁신형 제약 개발 신약인 대웅제약의 'DWP16001'으로 지난 2020년 10월 23일 동시 적용됐다.
신속심사 지정 신청은 구성성분, 작용기전, 제조방법, 해당 질환에서 임상적 의미가 있는 유효성을 확인할 수 있는 예비 임상시험 자료, 목표 적응증 등이 필요하며 지정 신청은 30일 내 검토 완료된다.
지난 2년간 신속심사 지정 후 허가 완료된 품목은 화학의약품 5품목, 생물의약품 1품목, 코로나19 백신 10품목, 생약 1품목으로 총 17품목이며, 일반심사기간의 75% 이내 심사 완료를 목표로 진행됐다.
2020년 8월 31일부터 올해 7월 31일까지 의료제품 신속심사 지정 신청은 총 25건으로 이 중 23건이 지정됐다. 지정신청 품목 중 1건은 기존 치료법 대비 유효성 개선 입증 자료 미흡으로 미지정됐으며, 1건은 자진 취하했다.
신속심사 지정 품목 중 생명을 위협하거나 중대한 질환 치료제는 12품목, 공중보건 위해 감염병 예방 또는 치료 의약품은 7품목, 혁신형 제약기업 개발 신약은 4품목으로 나타났다.
약효군별로 항악성종양제 56.5%(13품목), 코로나19 치료제 및 백신 30.4%(7품목), 화학요법제 4.3%(1품목), 순환기계의약품 4.3%(1품목), 당뇨병용제 4.3%(1품목) 다.
신속심사 품목허가 17품목 중 코로나19 백신이 10품목, 항악성종양제 5품목으로 높은 비중을 차지했다. 지정품목 중 8품목은 현재 심사가 진행 중이며, 허가 신청하지 않은 품목은 1건이다.
코로나19 백신의 신속심사 소요 일수는 평균 26근무일로, 백신을 제외한 품목은 평균 51근무일로 나타났다.
품목허가 신청 이전 허가기간을 단축할 수 있도록 하는 사전검토는 그동안 22건 이뤄졌다.
신속심사 수행 시 사전검토 제도를 활용한 수시동반심사의 경우 아스트라제네카, 화이자, 얀센 등 코로나19 백신 등이 신청하면서 심사를 진행했다.

식약처는 지난 2년간 신속심사 경험을 바탕으로 GIFT 프로그램을 시작할 예정이다.
GIFT 프로그램은 글로벌 혁신 의료제품이 신속하게 제품화될 수 있도록 개발(임상) 초기부터 지원하는 프로그램으로, 제약업체가 신속심사 대상 신청 시 지정을 검토하고 필요할 경우 의료제품 신속심사 전문가협의체 자문을 거쳐 GIFT 대상을 결정한다.
GIFT 대상은 ▲준비된 자료부터 먼저 심사하는 수시 동반심사(rolling review) 적용 ▲품목설명회·보완설명회 등 심사자와 개발사 간 긴밀한 소통 ▲규제 관련 전문 컨설팅 ▲혁신성(안전성·유효성 개선)이 뛰어난 제품은 임상 결과 등을 제공해 국내 의약품 개발 독려 ▲안전과 직접 관련 없는 일부 자료는 시판 후 제출 ▲ICH 등 글로벌 심사기준 선제적 적용 등 다양한 지원을 받게 된다.
http://www.dailypharm.com/Users/News/NewsView.html?ID=291752